Die Mikrotubuli des Zellskeletts trennen bei der Zellteilung die Chromosomen voneinander oder transportieren Zellorganellen und Bläschen mit Substanzen an ihren Bestimmungsort. Wie sie dabei immer die richtige Andockstelle finden, war bisher unklar. Jetzt haben Wissenschaftler eine Abfolge von vier Aminosäuren als den entscheidenden Marker am Ende der Mikrotubuli identifiziert. Ihre Ergebnisse sind jetzt in der Fachzeitschrift „Cell“ erschienen.
Eine lebende Zelle ist von einem dichten Geflecht von Polymerfasern durchzogen. Die drei Arten dieser Fasern durchziehen die Zelle und bilden gemeinsam das Zellskelett, zu dessen Aufgaben es gehört, die Zelle zu stabilisieren und in Form zu halten. Die Polymerfasern bilden aber kein steifes Gerüst, sondern reagieren flexibel auf äußere Einflüsse und sind aktiv an zahlreichen lebenswichtigen Vorgängen in der Zelle beteiligt. So können die Enden bestimmter Polymerfasern, der Mikrotubuli, Chromosomen, Zellorganellen und andere Zellbestandteile spezifisch erkennen und sich mit ihnen verbinden.
Zuständig dafür sind spezielle Proteine, die wie Greifer wirken – sie docken mit dem einen Ende an der Faser an, mit dem anderen halten sie das spezifisch erkannte Zellbestandteil. Dabei sind die verschiedenen Greiferproteine sehr unterschiedlich und kompliziert aufgebaut – und haben doch alle gemeinsam, dass sie sich mit dem Faser-Ende verbinden können.
Vier Aminosäuren passend aufgereiht
Ein besonders Mitglied dieser Klasse von Greiferproteinen ist das Protein EB1, das als einziges direkt an die Enden der Mikrotubuli andocken kann. Alle anderen Proteine können sich lediglich mit dem EB1 verbinden. Dabei war lange unklar, wie EB1 und die anderen Proteine zueinanderfinden. Diese Frage beantworten jetzt die Ergebnisse der Forscher von Paul Scherrer Institut und Erasmus Medical Center.
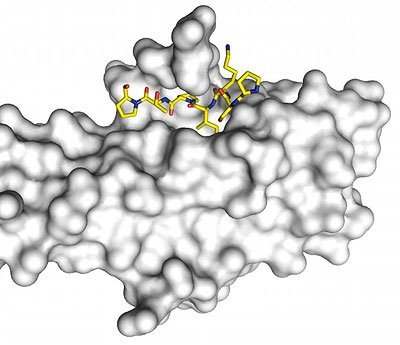
Die Forscher konnten nun zeigen, dass es einen sehr kleinen Abschnitt gibt, der all diesen Proteinen gemeinsam ist und ihnen erlaubt sich an das Faser-Ende einzuhaken. Dieser Abschnitt funktioniert wie eine Fahrkarte – wer ihn hat, kann auf dem Faser-Ende mitfahren. Sie konnten zeigen, dass allen diesen Proteinen eine bestimmte Abfolge von vier Aminosäuren gemeinsam ist.
Diese Sequenz hat dabei eine typische Form, die exakt in einen Freiraum in der Struktur des EB1 passt. So können die Proteine unabhängig von ihrer übrigen Form exakt an das EB1 und somit indirekt an die Enden der Mikrotubuli andocken. In der üblichen Nomenklatur wird diese Sequenz mit SxIP abgekürzt, wobei S für die Aminosäure Serin, I für Isoleucin und P für Prolin steht; x steht für eine beliebige andere Aminosäure.
Neue Medikamente möglich
„Dadurch dass Mikrotubuli an fast allen Vorgängen in der Zelle beteiligt sind – bis hin zur Trennung der Chromosomen während der Zellteilung – sind sie auch ein zentraler Angriffspunkt für Medikamente, die das Wachstum von Krebszellen aufhalten. Unsere Ergebnisse können somit helfen, neue Medikamente zu entwickeln, die gezielt in die von Mikrotubuli bestimmten zelluläre Prozesse
eingreifen.“ erklärt Michel Steinmetz, Leiter der Arbeitsgruppe Proteinwechselwirkungen am Paul Scherrer Institut und Initiator des Projekts eine mögliche Anwendung seiner Resultate.
Die Forschungs-Ergebnisse wurden erst durch eine Kombination von Methoden möglich – so wurde die dreidimensionale Struktur der beteiligten Proteine untersucht und deren Aminosäuresequenzen nach gemeinsamen Abschnitten abgesucht. Schliesslich konnte deutlich gezeigt werden, dass die Proteine
nicht mehr über EB1 an die Mikrotubuli-Enden binden können sobald die SxIP-Sequenz beschädigt ist. Am Paul Scherrer Institut ist das Gesamtkonzept des Forschungsprojekts entwickelt und sind die strukturellen Untersuchungen mittels Röntgenkristallographie an der Synchrotron Lichtquelle Schweiz SLS des Paul Scherrer Instituts durchgeführt worden.
Neben Forschern des Paul Scherrer Instituts und des Erasmus Medical Centers waren noch Wissenschaftler des Instituts für Molekulare Biologie der ETH Zürich und des Biochemischen Instituts der Universität Zürich an der Arbeit beteiligt.
(Pressemitteilung Paul Scherrer Institut (PSI), 27.07.2009 – NPO)