Der menschliche Körper muss sich ständig gegen Bakterien und Viren verteidigen. Zwar ist das Immunsystem auf solche Attacken gut vorbereitet: Sensoren in den Zellen identifizieren eindringende Bakterien und leiten daraufhin ein gezieltes Abwehrprogramm ein. Allerdings erschweren Viren dem Immunsystem die Erkennung, da diese nur ihre nackte Erbinformation in die Zellen schleusen. Nun sind Wissenschaftler einem Mechanismus auf die Spur gekommen, mit dessen Hilfe Sensoren in der Zelle virale Erreger dennoch aufspüren können.
{1r}
Die Forscher um Dr. Simon Rothenfusser vom Klinikum der Universität München (LMU) fanden heraus, dass virales Genmaterial zwei unterschiedliche Strukturmerkmale besitzt, die von einem Immunsensor erkannt werden. Die Ergebnisse sollen helfen, neuartige Therapien gegen Viren zu entwickeln – wie auch gegen Tumorleiden, berichten die Wissenschaftler in der Online-Ausgabe der Fachzeitschrift „Proceedings of the National Academy of Sciences“ (PNAS). In der Studie kamen rein synthetisch hergestellte Imitate viralen Erbmaterials zum Einsatz.
Viren als Freibeuter
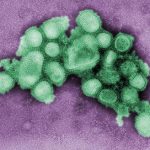
Die alljährliche Grippewelle im Winter zeigt eines ganz besonders deutlich: Den Angriffen von Viren ist der Mensch immer noch relativ schutzlos ausgeliefert. Meist gelingt es dem Körper erst nach einer mehr oder weniger schweren Krankheitsphase, sich gegen den Eindringling zu wehren und die Krankheit zu überwinden. Diese Erreger sind für die Körperabwehr so schwer zu fassen, weil sie – anders als Bakterien – ihre spezifischen Oberflächenmerkmale, die von Immunsensoren des Körpers erkannt werden, abstreifen können.
Viren sind so etwas wie mikroskopisch kleine Freibeuter: Sie lassen beim Eindringen in die Zelle ihre Hüll- und Kapselstrukturen zurück und schleusen nur ihre nackte Erbinformation, die DNA oder RNA, in die Körperzellen ein.
Erreger deponieren Kuckucksei
„Die genetischen Informationen des Menschen und der Viren sind in ihrer Struktur fast oder ganz identisch aufgebaut“, erklärt Rothenfusser. „Viren können ihre RNA-Moleküle daher in einer Zelle wie ein Kuckucksei deponieren. Erkennt die Zelle die subtilen Besonderheiten des fremden Materials nicht, liest sie in der Folge die Gene des Virus wie ihre eigenen ab und produziert so ständig neue Virusnachkommen.“
Wenn der Körper die virale Erbinformation nicht als fremdes Material erkennt, können die wirksamen Abwehrprogramme des Immunsystems aber nicht aktiviert werden, die die Vermehrung und Verbreitung der Eindringlinge meist erfolgreich unterbinden.
Molekularer Sensor identifiziert
In seiner neuen Studie konnte das Team um Rothenfusser nun zeigen, anhand welcher Merkmale ein im Zellinneren gelegener Immunsensor virale RNA erfolgreich von zelleigener RNA unterscheiden kann. Dieser molekulare Sensor namens RIG-I – retinoid acid inducible gene I – hat sich als wesentlicher Faktor bei der Abwehr des Grippevirus und des Erregers der Hepatitis C erwiesen.
Er besitzt die Fähigkeit, in die Zelle eingedrungene virale RNA zu erkennen und löst daraufhin eine Abwehrreaktion aus, die das Virus heftig attackiert. Um diese Aufgabe zu leisten, muss das Virus zwei von der Sequenz der RNA unabhängige Struktureigenschaften besitzen, fand die Gruppe um Rothenfusser in Zusammenarbeit mit Professor Karl-Peter Hopfner vom Genzentrum der LMU jetzt heraus.
RIG-I entlarvt Virus
Erstens muss das RNA-Molekül an einem Ende, dem so genannten 5′-Ende, eine frei zugängliche chemische Variation besitzen: das 5′-Triphosphat. Zweitens muss die Virus-RNA über mindestens sieben bis zehn aufeinanderfolgende Basen, das sind die Grundbausteine des Erbmaterials, eine doppelsträngige Struktur ausbilden. Die Kombination beider Eigenschaften kommt bei der zelleigenen RNA im Zytoplasma nicht vor und ist so ein eindeutiges Erkennungsmerkmal. Um die verschiedenen Virusmerkmale zu erkennen, sind zwei unterschiedliche Bereiche von RIG-I zuständig, wie die Untersuchungen der Forscher ergaben.
„Wir nehmen an, dass RIG-I die Informationen über beide Merkmale integriert und erst dann eine antivirale Abwehrreaktion auslöst“, sagt Dr. Andreas Schmidt, Erstautor der Veröffentlichung. Zwar gibt es Viren, die entweder das eine oder das andere Merkmal nicht aufweisen und so schwer zu identifizieren sind. Sind aber beide Besonderheiten vorhanden, kann RIG-I das Virus eindeutig „entlarven“.
Charakteristische Verunreinigungen
Somit ist es den Forschern gelungen, ein Profil viraler RNA zu definieren, das ausreichend für die Aktivierung von RIG-I ist. Die getrennte Untersuchung der beiden Virusmerkmale gelang ihnen, weil sie durch Zusammenarbeit mit der Biotech-Firma Eurogentec erstmals vollständig synthetisch hergestellte und somit exakt definierte 5 ‚-Triphosphat-RNA zur Verfügung hatten, die keinerlei Verunreinigungen enthielt.
Auf herkömmlichem Weg mithilfe von Enzymen hergestelltes 5′-Triphosphat zeigt dagegen charakteristische Verunreinigungen mit nicht kontrollierbaren RNA-Stücken, die häufig zu widersprüchlichen Ergebnissen führten.
Synthetische Imitate von Viren-RNA
Die neuen Erkenntnisse könnten es in Zukunft nach Angaben der Forscher auch erlauben, vollständig synthetische Imitate von Viren-RNA herzustellen, um so möglicherweise bei der Entwicklung von Medikamenten das Immunsystem gezielt stimulieren. „Wir hoffen, auf diese Weise neue therapeutische Ansätze zur Behandlung von Tumoren und chronischen Virusinfektionen zu finden“, so Rothenfusser.
Eine mögliche Anwendung ist, auf synthetischem Weg RNA-Moleküle herzustellen, die sowohl doppelsträngige Abschnitte als auch ein modifiziertes 5′-Triphosphat enthalten. Diese Moleküle können so gestaltet werden, dass sie gleichzeitig in der Lage sind, über den Mechanismus der RNA-Interferenz zelleigene Gene auszuschalten und eine Virus-RNA zu imitieren – so dass sie über RIG-I eine Antwort des Immunsystem provozieren.
Neuer Ansatz im Tiermodell erfolgreich
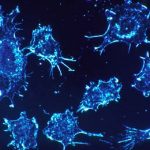
„Dieser neue Ansatz ließ sich im Tiermodell bereits erfolgreich zur Therapie von Melanomen, also bösartigem Hautkrebs, einsetzen“, berichtet Rothenfusser. In Zukunft wollen die Forscher den neuartigen Ansatz in seinen Anwendungsmöglichkeiten weiter untersuchen.
(idw – Universität München, 07.07.2009 – DLO)