Die altersbedingte Makula-Degeneration (AMD) ist die Hauptursache für Erblindungen von Erwachsenen. Bisher nicht heilbar, wurde sie aus Mangel an guten Früherkennungsverfahren oft zu spät erkannt. Jetzt aber haben Forscher einen Marker und Schlüsselakteur für das krankhafte Einwachsen von Blutgefäßen in die Netzhaut identifiziert. Damit ist nicht nur eine frühere Erkennung, sondern zukünftig auch eine bessere Behandlung möglich, wie die Wissenschaftler in „Nature“ berichten.
{1l}
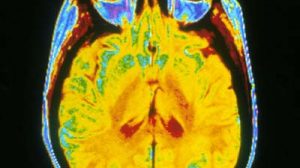
Weltweit sind 25 bis 30 Millionen Menschen an einer altersbedingten Makuladegeneration erkrankt, in Deutschland sind zwei Millionen betroffen. Sie gilt als Hauptursache für Erblindungen Bei dieser bisher nicht heilbaren Krankheit wuchern Blutgefäße in die Netzhaut ein und lösen letztlich den Verlust der Sehkraft an der Stelle des schärfsten Sehens, der Makula, aus.
„Wenn die Gefäße einmal in die Netzhaut eingedrungen sind, ist der Schaden schon passiert“, erklärt Jayakrishna Ambati von der Universität von Kentucky. „Zu diesem Zeitpunkt können Wirkstoffe zwar das Fortschreiten verlangsamen, aber meist ist bereits irreparabler Schaden angerichtet. Deshalb ist es so wichtig, Möglichkeiten der Früherkennung und Intervention zu finden.“ Gemeinsam mit Kollegen hat Ambati nun einen Rezeptor identifiziert, der sich als Marker für eine Früherkennung eigenen könnte.
CCR3-Rezeptor nur auf krankhaften Gefäßen vorhanden
Die Wissenschaftler entdeckten, dass CCR3, ein Rezeptor-Molekül, das auch an zahlreichen Entzündungsprozessen beteiligt ist, auf der Oberfläche der in bei AMD die Netzhaut einwachsenden Gefäße vorhanden ist. Bei normalen Blutgefäßen fehlt dieser Rezeptor dagegen. Entdeckt wurden die Rezeptoren mithilfe von winzigen Halbleiter-Nanokristallen, die die Forscher als Vehikel für Anti-CCR3-Antikörper in das Auge von Mäusen injizierten.
Die Antikörper binden an die auf den abnormalen Gefäßen sitzenden Rezeptoren. Durch ihr anhängendes Nanovehikel machen sie diese mit konventioneller okularer Angiographie sichtbar – und dies sogar bevor die krankhaften Gefäße in die Netzhaut eingewandert sind. Bisher war es nur möglich, die bereits eingedrungenen Gefäße sichtbar zu machen, doch dann war der Schaden bereits geschehen.
Früherkennung schon vor dem ersten Schaden
„Der CCR3-Rezeptor ist bereits als Schlüsselakteur im allergischen Entzündungsprozess bekannt“, so Grace Shen, Leiterin der Augenimmunologie am National Eye Institute der USA. „Ambatis Studien haben nun CCR3 auch als entscheidenden Marker des Gefäßneubildungsprozesses bei AMD enthüllt.“
Ihr Kollege Stephen J. Ryan, Professor für Augenheilkunde an der Universität von Südkalifornien ergänzt: „Das ist eine aufregende Entdeckung für Millionen Menschen, die das Risiko besitzen, an feuchter AMD zu erkranken. Die neue Bildgebungstechnologie gibt uns die Möglichkeit, pathologische Gefäßneubildungen zu entdecken bevor sie die Netzhaut schädigen und einen Verlust der Sehkraft auslösen.“
Bessere Therapien in Aussicht
Das Forscherteam entdeckte nicht nur, dass CCR3 eine einzigartige Signatur für die Gefäßneubildung darstellt, sie fanden auch heraus, dass das Gen für diesen Rezeptor das anormale Wachstum der Gefäße im Auge aktiv fördert. Die Antikörper, die eingesetzt werden, um die krankhaften Wucherungen zu entdecken könnte daher möglicherweise sogar auch als Therapie eingesetzt werden.
Die ersten Ergebnisse sind vielversprechend: Eine Behandlung mit Anti-CCR3-Antikörpern reduzierte die pathologische Gefäßneubildung bei Mäusen um rund 70 Prozent. Herkömmliche Behandlungsmethoden erreichen zurzeit nur eine Quote von 60 Prozent. Nach Ansicht von Ambati sind klinische Studie der Phase 1 nicht mehr weit entfernt.
„Die Identifikation des CCR3 auf den Endothelzellen der anormalen Gefäße in AMD ist ein großer Durchbruch“, so Patricia A. D’Amore, Professorin für Augenheilkunde an der Harvard Medical School. „Die präklinischen Daten sind sehr spannend und deuten darauf hin, dass CCR3 die Basis der nächsten Generation von gezielten Angiogenesehemmern für die feuchte AMD sein könnte.”
(University of Kentucky, 17.06.2009 – NPO)