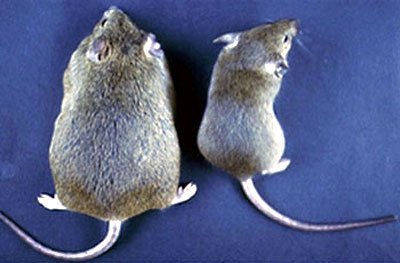
Die Fettregulation im Körper ist sehr komplex: Das Gehirn spielt eine wichtige Rolle dabei und passt die Nahrungsaufnahme an den tatsächlichen Energieverbrauch an. Neu ist, dass auch Nerven, die außerhalb des Gehirns und des Rückenmarks liegen, an diesem fein abgestimmten Prozess beteiligt sind. Das haben jetzt Forscher herausgefunden. Den entscheidenden Hinweis lieferten gentechnisch veränderte Mäuse, bei denen das Gen Nscl-2 ausgeschaltet worden war.
Dieses ist nach Angaben der Wissenschaftler vom Max-Planck-Institut für Herz- und Lungenforschung in Bad Nauheim sowie der Universitäten Halle, Leipzig und Berlin normalerweise nur in Nervenzellen aktiv. Mäuse, denen Nscl-2 fehlte, entwickelten eine massive Fettleibigkeit – Adipositas -, blieben jedoch von Folgeschäden wie der Zuckerkrankheit (Diabetes) weitgehend verschont.
Die neue Entdeckung könnte langfristig auch Adipositas-Patienten helfen, die an Diabetes leiden, berichten die Forscher in der Fachzeitschrift „PLoS One“.
Zu viele Kalorien machen dick
Wer auf Dauer zu viele Kalorien aufnimmt, wird dick. Hinter diesem einfachen Zusammenhang verbergen sich komplexe Mechanismen, die den Energieverbrauch messen und die Nahrungsaufnahme daran anpassen. Die Steuerungszentrale liegt in einem bestimmten Teil des Gehirns, dem Hypothalamus. Vor allem die heutige kalorienreiche Ernährung kann jedoch bewirken, dass die Steuerung aus dem Lot gerät – die Folge ist Fettleibigkeit.
Thomas Braun vom Max-Planck-Institut für Herz- und Lungenforschung und sein Team fanden nun heraus, dass an der Entstehung von Adipositas nicht nur das Gehirn, sondern auch das Fettgewebe selbst beteiligt ist – genauer gesagt die Nerven, die im Gewebe liegen.
Weniger Nerven im Fettgewebe
Auf die Spur dieser Erkenntnis brachten die Forscher Mäuse, bei denen ein bestimmtes Gen, das so genannte Nscl-2, ausgeschaltet worden war. Das Gen ist sonst ausschließlich in Neuronen aktiv. Bei Mäusen, denen Nscl-2 fehlte, fanden die Forscher im Fettgewebe deutlich weniger Nerven. Besonders die kleinen Nervenfasern sowie diejenigen des vegetativen Nervensystems fehlten. Dadurch war die Informationsübertragung im Fettgewebe bei diesen Tieren deutlich reduziert.
Da Nervenfasern normalerweise entlang kleiner Blutgefäße, den Kapillaren, verlaufen, vermutete Braun einen Einfluss auf das Kapillarnetzwerk. „Erst seit Kurzem ist bekannt, dass Gefäß- und Nervensystem intensiv miteinander kommunizieren. Deshalb überraschte es uns nicht, als wir sahen, dass im Fettgewebe nicht nur Nervenfasern fehlen, sondern auch viel weniger Kapillaren vorhanden sind“, sagt der Forscher.
Hohe Zahl unreifer Fettzellen
Spannend war nun die Frage, ob und wie sich die Zusammensetzung des Fettgewebes zwischen Wildtyp-Mäusen und solchen, denen Nscl-2 fehlte, unterschied. „Auffällig ist, dass der Anteil unreifer ‚kleiner‘ Fettzellen bei den Nscl-2-defizienten Mäusen um den Faktor 7 erhöht ist“, stellt Braun fest. Vor allem ein Subtyp dieser Fettzellen (Adipozyten), den die Forscher im Gewebe von Wildtyp-Mäusen überhaupt nicht fanden, konnten sie bei Nscl-2-defizienten Mäusen in großer Zahl nachweisen.
Wie die Max-Planck-Wissenschaftler vermuten, ist die erhöhte Anzahl unreifer Fettzellen dafür verantwortlich, dass es den übergewichtigen Tieren vergleichsweise gut geht, obwohl sie aufgrund ihrer Fettsucht eigentlich einen Typ II-Diabetes entwickeln müssten.
Kein direkter Nutzen für Adipositas-Patienten?
Einen direkten Nutzen für Adipositas-Patienten verspricht sich Braun von den Ergebnissen derzeit jedoch nicht. Die Tatsache, dass die Mäuse mit dem fehlenden Ncsl-2 zwar nach der Pubertät fett werden, aber entgegen der Erwartung keine Typ II Diabetes entwickelten, weckt bei den Wissenschaftlern aber die Hoffnung, dass Betroffene auf lange Sicht von der Entdeckung des neuen Mechanismus doch profitieren werden.
So wäre es denkbar, mittels des jetzt aufgedeckten Mechanismus Einfluss auf die Reifung von Fettzellen zu nehmen, um damit die Stoffwechselregulation zu verbessern.
(idw – MPG, 16.06.2009 – DLO)