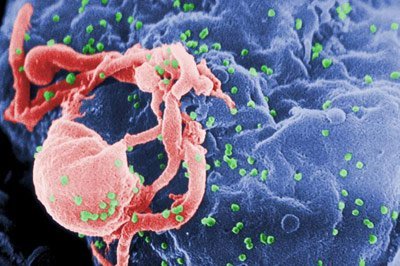
Für Aufsehen sorgte 1997 die Entdeckung eines französisch-britischen Forscherteams um Hervé Perron. Die Wissenschaftler hatten in der Rückenmarksflüssigkeit von Patienten mit der Autoimmunerkrankung Multiple Sklerose (MS) die Signatur eines Virus nachgewiesen, das sich als endogenes Retrovirus entpuppte. Das env-Gen dieses HERV-W war genau die Sequenz, die auch das für die Plazenta so wichtige Protein Syncytin-1 produzierte. Aber war diese Genaktivität wirklich der Auslöser der MS? Immerhin war ja auch bereits in den Gehirnen gesunder Menschen Syncytin gefunden worden.
Syncytin als Januskopf
Zahlreiche Forschergruppen sprangen auf den Zug auf und suchten nach Zusammenhängen. Im Jahr 2004 gelang es dann einem internationalen Team von Wissenschaftlern tatsächlich, das HERV-W mindestens als mitschuldig zu überführen. Sie hatten nicht nur das Virenprotein genau am Ort des Geschehens nachgewiesen, sondern auch, welche Folgen seine Präsenz dort hat:
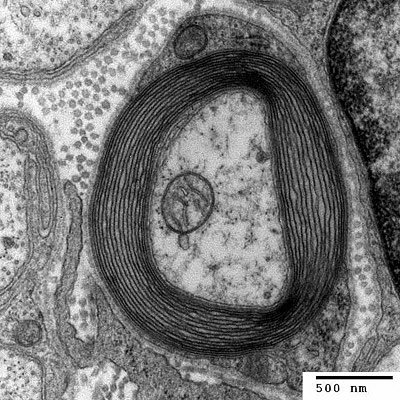
„Das Syncytin-1 wird dabei genau in den Regionen der akuten Demyelinisierung gebildet“, schildert „Virolution“-Autor Frank Ryan die Ergebnisse. „Und es kann beim besten Willen nicht mehr als Schutzfaktor gedeutet werden, denn es ruft die Freisetzung chemischer Verbindungen hervor, die die Oligodendrozyten abtöten, also jene Zellen, die die Myelinscheide bilden.“ Noch immer allerdings bleiben einige Fragen offen, darunter auch, warum das Syncytin bei MS-Patienten schädlich wirkt, sonst aber offensichtlich nicht. Könnte es mehrere Syncytinformen geben? Oder spielen möglicherweise weitere, exogene Einflussfaktoren eine Rolle?
HERV-Mitschuld auch bei Lupus?
Ein anderer Fall, bei dem Forscher heute zumindest eine Beteiligung endogener Retroviren vermuten, ist die Autoimmunerkrankung Lupus erythematodes (SLE). Bei dieser reagiert das Immunsystem der Betroffenen auf ungenügend abgebaute Relikte von Zellen, die eigentlich durch das körpereigene Selbstmordprogramm beseitigt werden sollten. Dies führt zu Hautveränderungen und Entzündungen in Gefäßen und Organen, die im Extremfall zum Organversagen und zum Tod führen können.
Neuere Untersuchungen haben nun gezeigt, dass die Blockade des Gens Trex1, das ein Enzym für die normale Entsorgung von DNA-Resten aus dem Zellkern kodiert, im Tierversuch Lupus auslösen kann. In den Zellen mit gestörter Trex1-Funktion finden sich wiederum ungewöhnlich viele Produkte endogener Retroviren. Ob dies allerdings Ursache oder Folge der Trex1-Blockade ist, bleibt bisher unklar. Es wird jedoch nicht ausgeschlossen, dass HERVS zumindest mit an der überschießenden Autoimmunreaktion beteiligt sind.
Kooperation unter Viren
In manchen Fällen können auch unvollständige oder vermeintlich „tote“ retrovirale Sequenzen unerwartete Aktivität entfalten: Wenn sie mit anderen, von außen eingedrungenen Viren in Kontakt kommen. Exogene und „hauseigene“ virale Gene helfen sich dann unter Umständen gegenseitig mit fehlenden Bausteinen aus und erzeugen so fatale Synergieeffekte.
In Laborversuchen haben Wissenschaftler beispielsweise bereits nachgewiesen, dass eine Infektion mit dem Epstein-Barr-Virus das endogene Retrovirus HERV-K18 in den befallenen B-Lymphozyten unseres Immunsystems aktiviert. Dieses produziert daraufhin ein „Superantigen“, das dem exogenen Erreger Vorteile gegenüber der Immunabwehr verschafft. Ähnliche Interaktionen könnten möglicherweise auch beim Aidserreger HIV vorkommen.
Kreative Kraft oder unfreiwilliger Usurpator?
Bei allen negativen Auswirkungen steht für Ryan und Villarreal vor allem die kreative und damit in der Evolution vorantreibende Kraft der Viren im Vordergrund. Für sie ist klar, dass auch die durch endogene Viren verursachten Genschäden oder Krankheiten eher ein „Unfall“ als Absicht oder Zweck der Übung sind. Letztlich überwiegt jedoch – zumindest für unsere Art als Ganzes –, der positive Effekt, die Entwicklungssprünge in unserer Stammesgeschichte, die wir diesen „blinden Passagieren“ verdanken.
Andere Wissenschaftler sind allerdings durchaus skeptischer und halten in der Summe die Folgen der retroviralen Kolonisierung eher für negativ. Sie sehen darin eher eine unfreiwillige „Übernahme“ als eine echte Symbiose. Wer am Ende Recht behält, werden weitere Studien zeigen – und letztendlich auch der weitere Verlauf der Evolution.
Nadja Podbregar
Stand: 05.11.2010